モニタリング
専門性と効率性を高め、変化の一歩先を目指すモニタリング業務
グローバルに医薬品開発を競い合う時代となり、治験や臨床研究を取り巻く環境は常に変化しおり、試験デザインも複雑化しています。弊社ではこうした変化を的確に捉え、常に一歩先を行くモニタリングへの挑戦を続けています。 最新の臨床開発業務経験や独自の情報網に基づき、実施医療機関のご提案から、臨床試験のモニタリング業務、非盲検モニタリング業務、クオリティマネジメント(QM)業務や臨床試験実施に関するコンサルティングなどトータルサービスを展開するとともに、ライフサイエンス分野のプロフェッショナルとして、常にCRA(Clinical Research Associate:臨床開発モニター)の能力・知識の向上を図り、高度なご要望にも的確にお応えすることができるよう心がけています。
弊社の取り組み
- 機能の分化、集約による高品質・高効率なモニタリングおよび関連業務の遂行
- グローバル査察に求められるALCOA※原則に基づいたモニタリング
- プロセスQMメソッドに基づく最適品質の保証
- ITのアドバンテージを活かしたeSource Data等への取り組み
- 専任の独立した部署による非盲検モニタリングの遂行
※ALCOA:治験データの品質を保証するために求められる原資料の残し方の基本原則で、以下の頭文字からきています。 1) Attributable(帰属/責任の所在が明確である)2) Legible(判読/理解できる) 3) Contemporaneous(同時である)4) Original(原本である)5) Accurate(正確である)
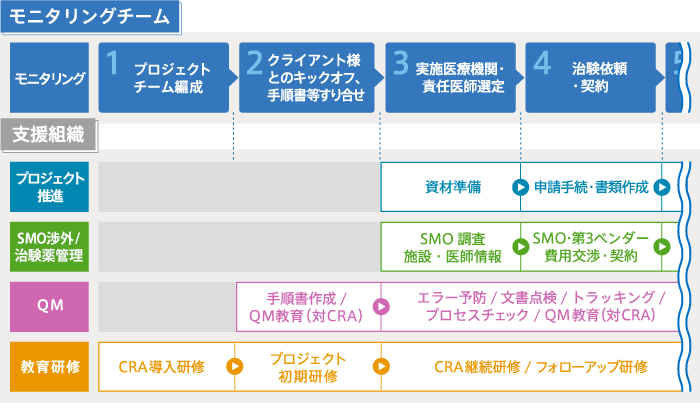
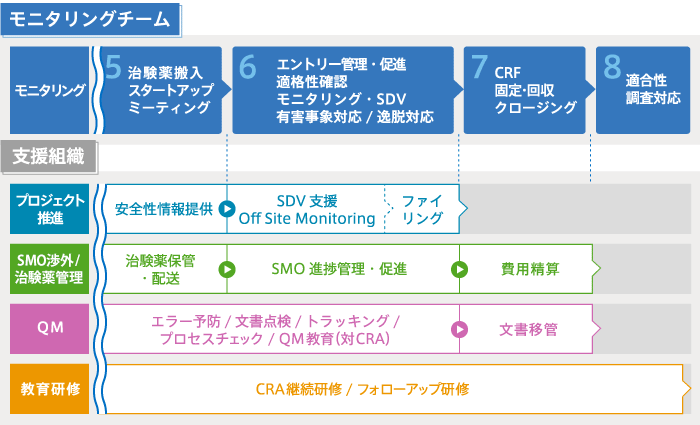
業務フロー
機能を分化・集約させた各支援組織がモニタリングチームを支えています。これによりCRAはGCPが意図する本来のモニタリング活動に集中でき、高品質・高効率なモニタリング業務が可能となります。
専門教育
モニタリング担当者の業務に必要な知識、技能の習得と向上を目標として、様々な研修を年間を通じて実施しています。
- CRA未経験者に対する初期導入及びフォローアップ研修カリキュラム
- 関連法規や疾患知識など、最新のトピックを反映した豊富な研修カリキュラム
- プロジェクト毎の初期導入・継続研修
- 上記の他、英語、リーダーシップ、マネジメントなど、ビジネススキル研修も実施
Expert制度
事前に定めた定義/要件を満たす者をSenior Expert、Expert、Junior Expertの3クラスで評価/認定します。高い専門性を基に担当業務において更なる質の向上と高付加価値を有するサービスを提供します。
社内においては教育研修にも積極的に関与することで次世代のExpertを計画的に育成します。
Expert制度は、オンコロジー、CNS、再生医療、医療機器、Global Study、Dermatology、臨床薬理の7制度があり、各領域等において、真のプロフェッショナルとして、医薬・医療の発展と全ての人々のQOL向上に貢献していきます。
