品質マネジメント/TMFマネジメント
主な業務内容
モニタリング業務の最適な品質を保証するために、以下に記載した品質マネジメント業務を実施しています。
- 手順書及び品質マネジメント計画の作成
- GCP等規制要件に関する継続的なCRA教育、アドバイス
- QMSに基づくGCP等規制要件及び依頼者要求事項に関するリスクマネジメント
- ドキュメントマネジメント
- プロセスマネジメント(GCP等規制要件及び各種手順書に基づいたプロセスの管理活動)
- ナレッジマネジメント(GCP等規制要件/モニタリング事例の収集分析/提案/改善活動)
- イシューマネジメント(モニタリング業務に関するイシューの収集/分析/提案/改善活動)
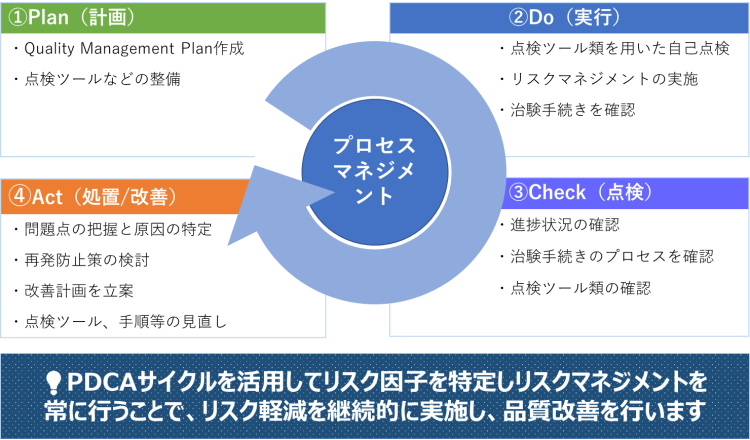
プロセスマネジメント及びドキュメントマネジメント
リーダー、CRA、QM担当者が三位一体となり、それぞれの立場での品質管理を行います。GCP要件や依頼者要求事項等からプロジェクトにおけるリスクを抽出し、エラーを最小限にするためのリスクマネジメント活動を実施します。モニタリングチームと試験成功に向けて協働することで、適合性書面調査に耐えうる最適な品質を確保していきます。
TMF Management
治験関連文書(Trial Master File, TMF)の管理は、承認申請における規制当局の要求事項を満たし、第三者に対し治験の実施経過の過程を説明可能にするための重要な要素です。
近年治験関連文書の管理手法としてeTMFを用いた電子文書管理が浸透しています。エイツーヘルスケアではお客様指定のeTMFシステムの仕様や要求事項に従い、最適なTMF Managementプロセスを構築し運用いたします。
既にeTMF導入済みのお客様、これからeTMF導入をご検討のお客様に以下のサービスをご提供いたします。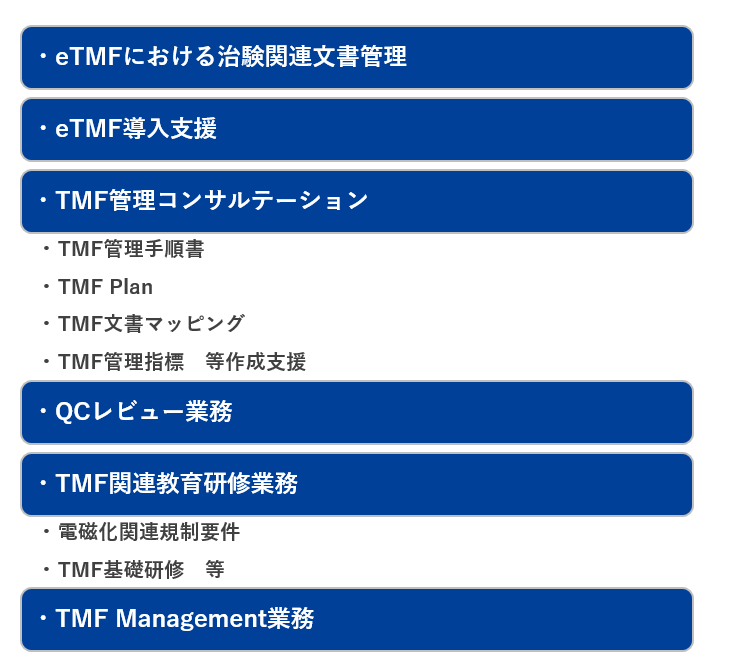
A2が考える TMF Management スタイル
■なぜeTMFなのか?
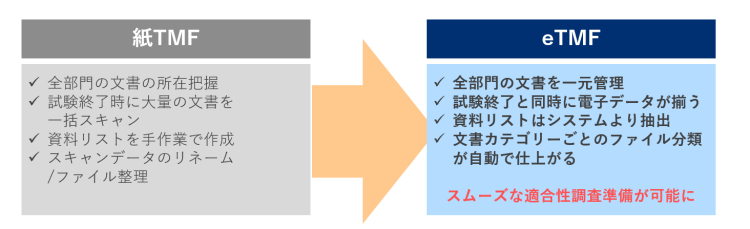
eTMFにより治験に関わる各組織のTMFを横断的に管理し、定期的なeTMFデータの確認を行うことで、いつでも調査・査察に耐えられる「Inspection Readiness」を達成することが可能です。これにより将来的な適合性調査準備にかかる文書整理の工数削減・準備期間の短縮を見込めます。また検索性の面でも、登録データから目的の資料・データを即時に検索することが可能であることも大きなメリットの1つとなります。

■紙から電子化へ
■TMF Managementプロセス
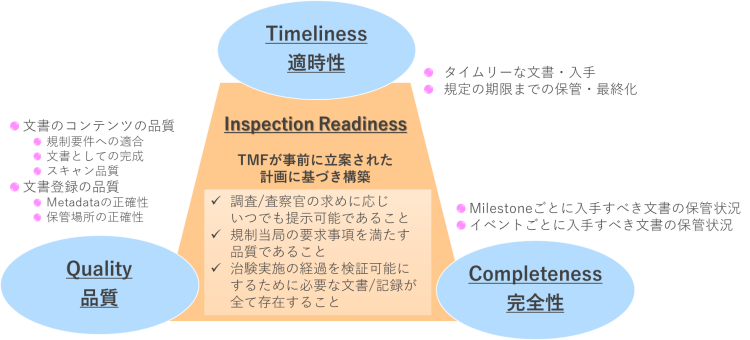
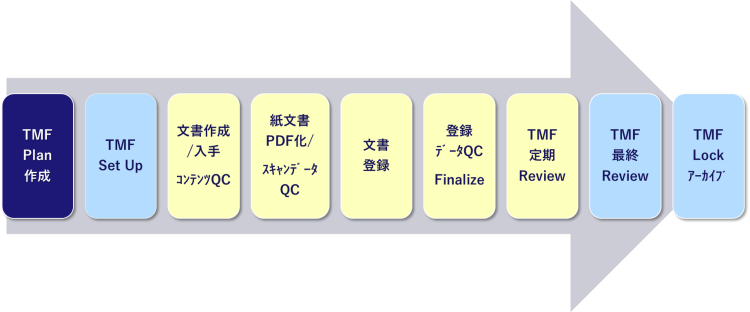 ■Inspection Readinessのための要素と指標管理の観点
■Inspection Readinessのための要素と指標管理の観点
TMF Managementの目的である「Inspection Readiness」を達成するため、eTMFデータを用いた指標管理を行い、TMFの適切な状態を維持します。